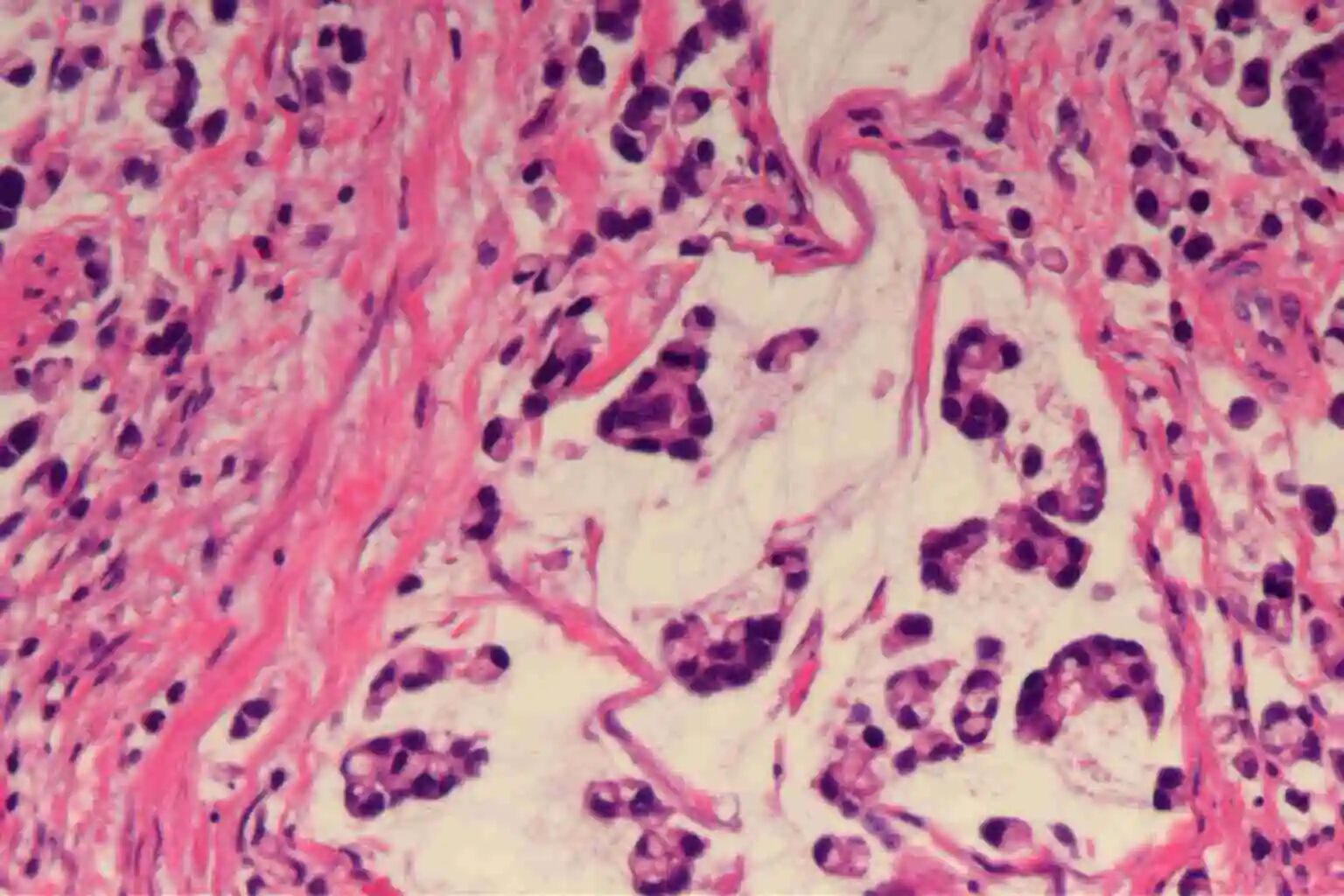
讲座|乳腺原发性腺样囊性癌1例介绍

患者,女,73岁,左乳肿物3年余,于2026年1月21日于我科住院期间行乳腺穿刺活检提示:(左乳肿物穿刺)(左侧)乳腺:符合腺肌上皮肿瘤,倾向于实性结节状恶性腺肌上皮瘤,穿刺组织有限,且该类肿瘤罕见,建议专科医院进一步确诊。免疫组化:ER(-),PR(-),CK5/6(+),Her-2(2+),Ki67(约20%+),E-Cadherin(+),P63(肌上皮+),Calponin(肌上皮+)。外院会诊后考虑非典型腺肌上皮瘤。患者要求手术治疗,病程中饮食睡眠尚可,二便如常,无心慌、胸闷不适,近期体重无明显下降。
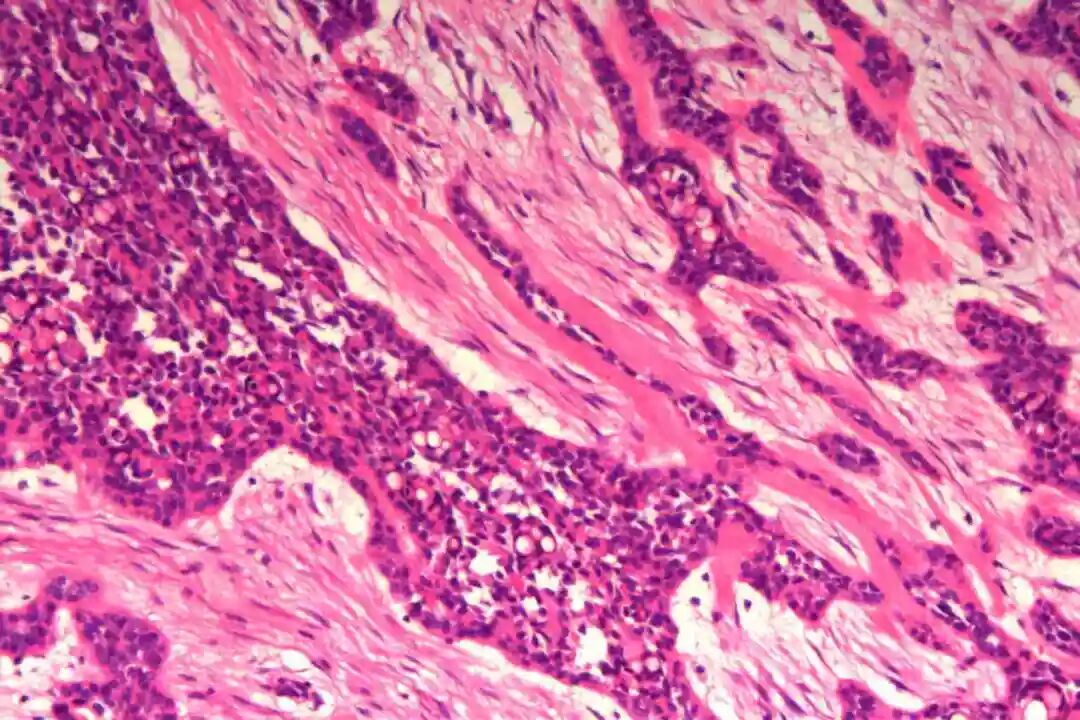
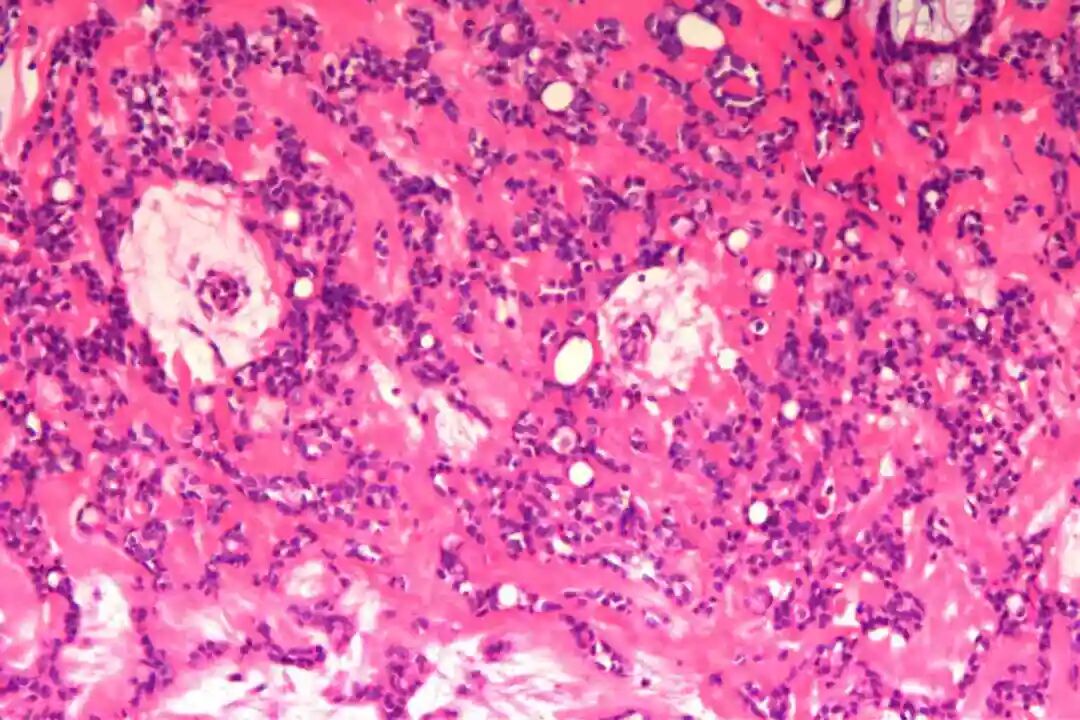
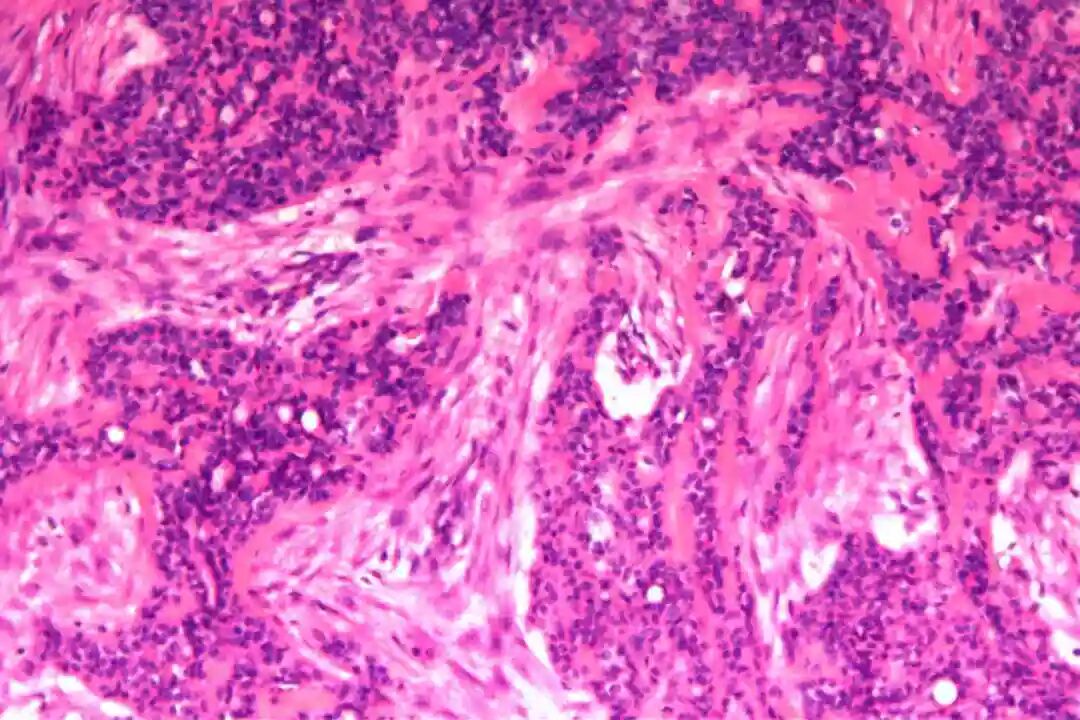
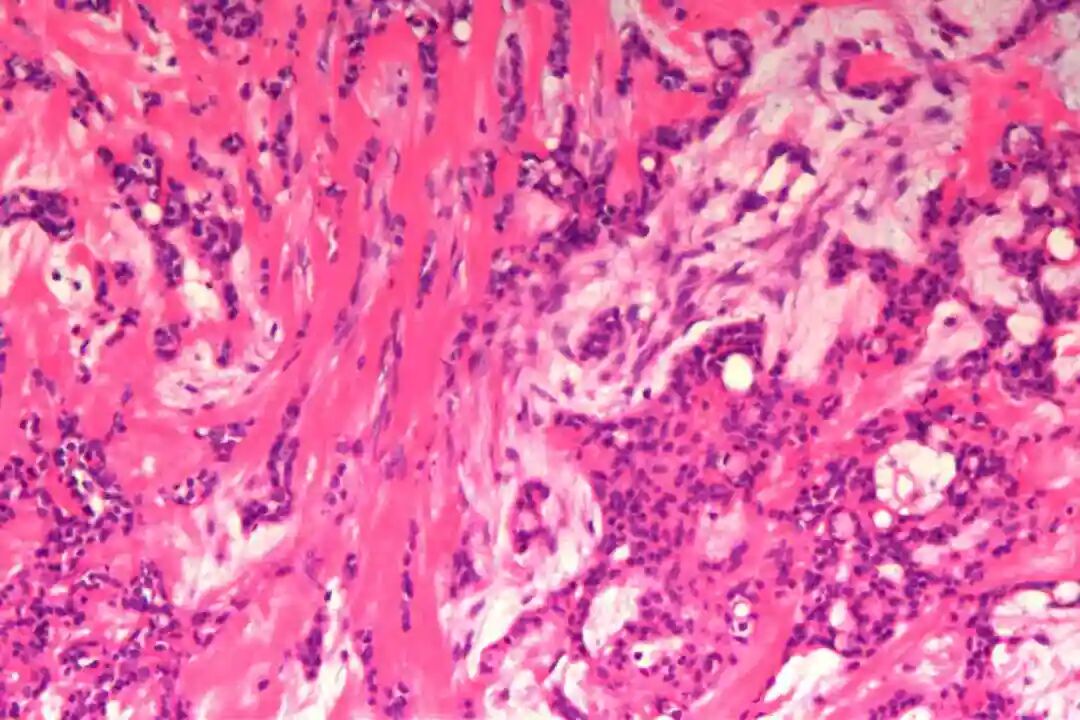
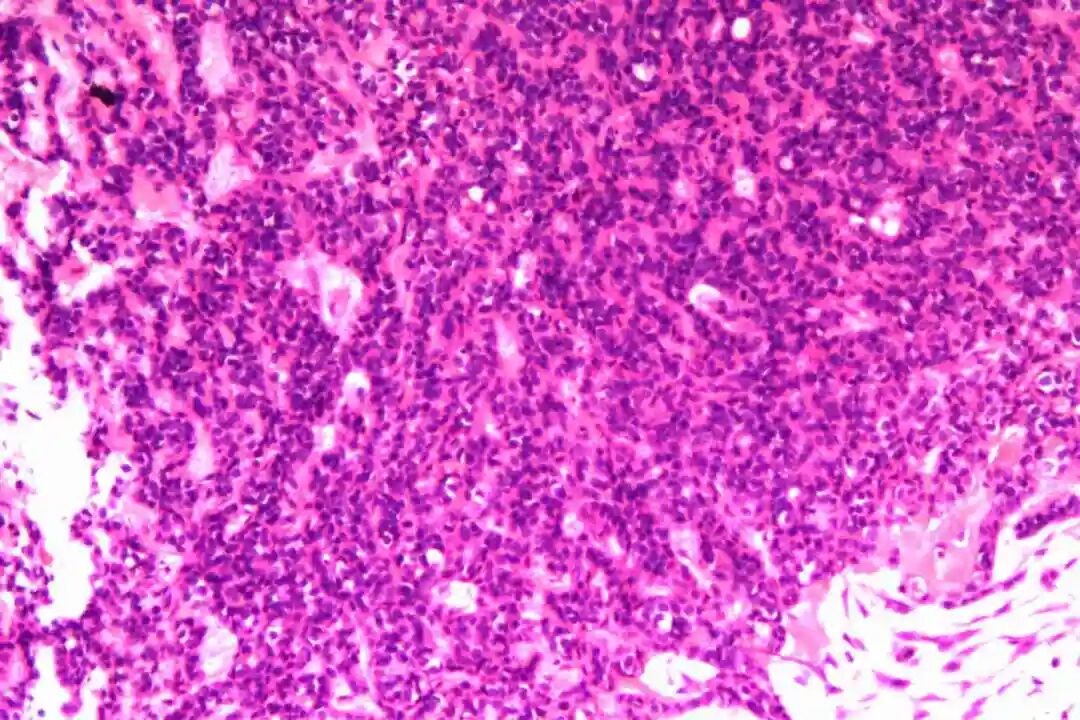
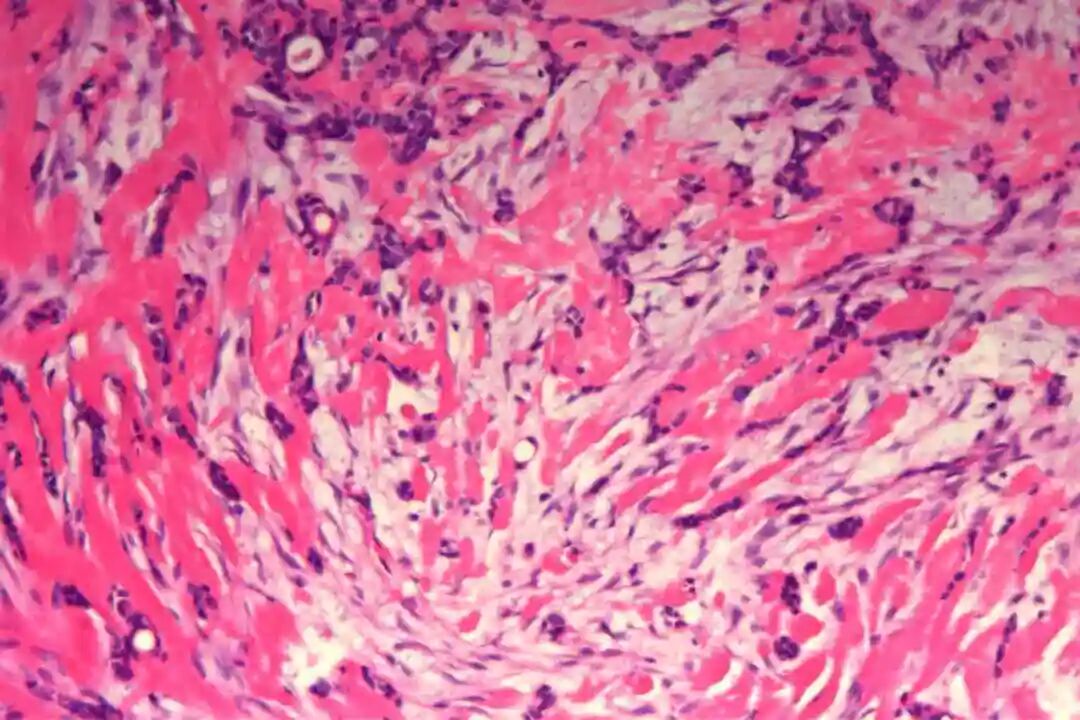
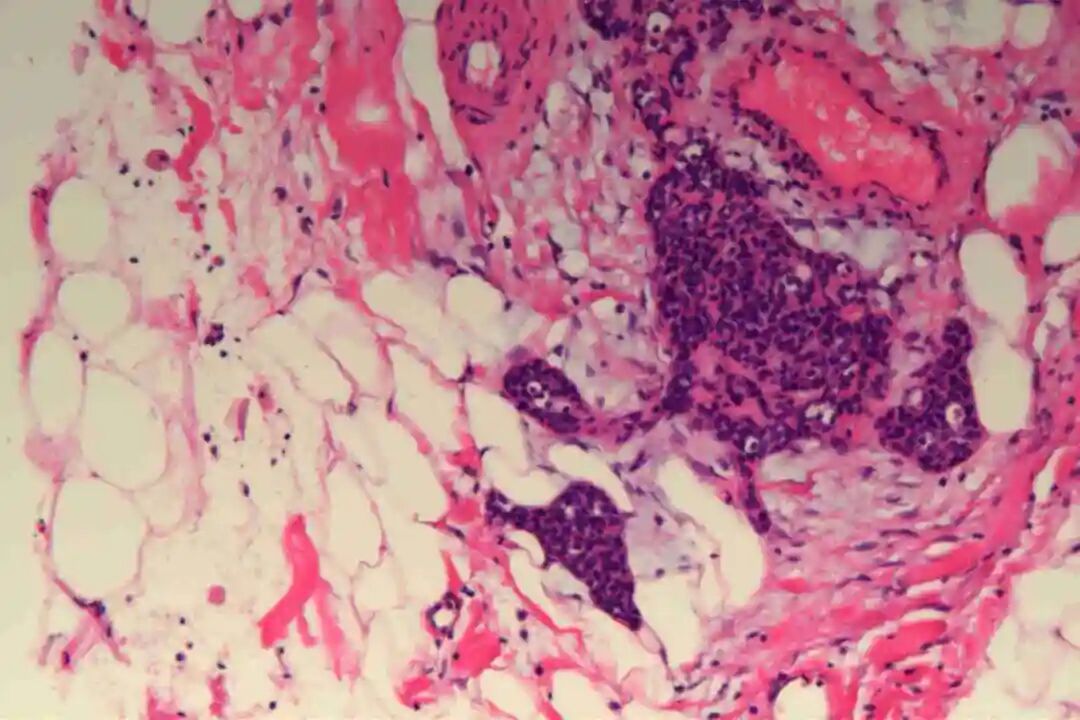
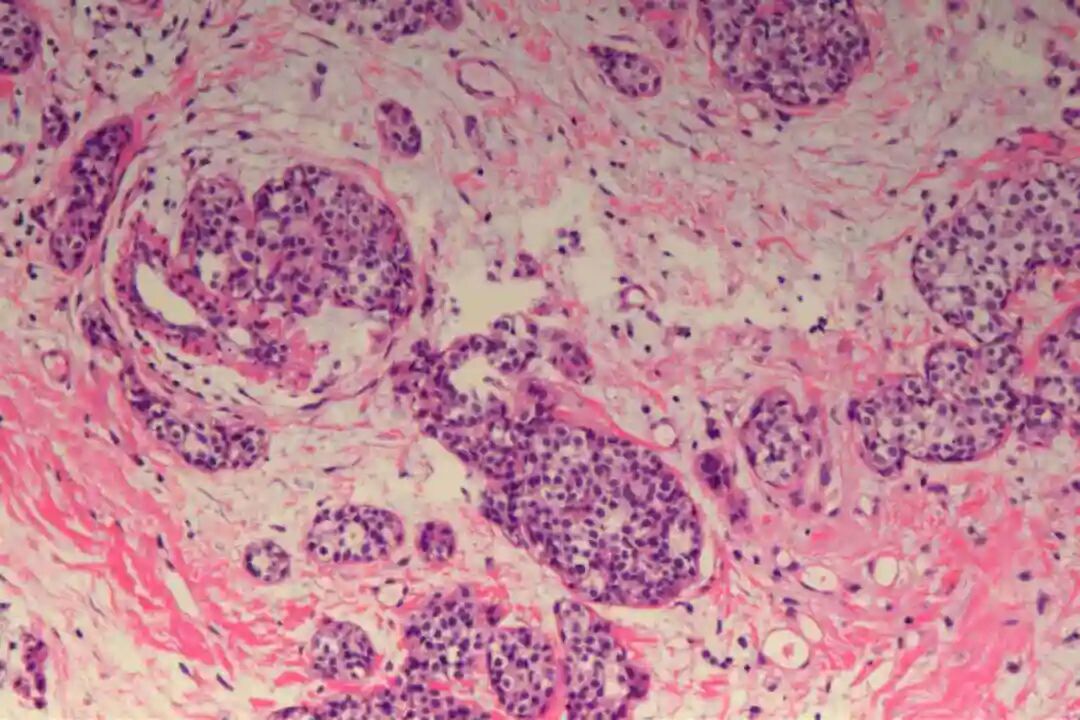
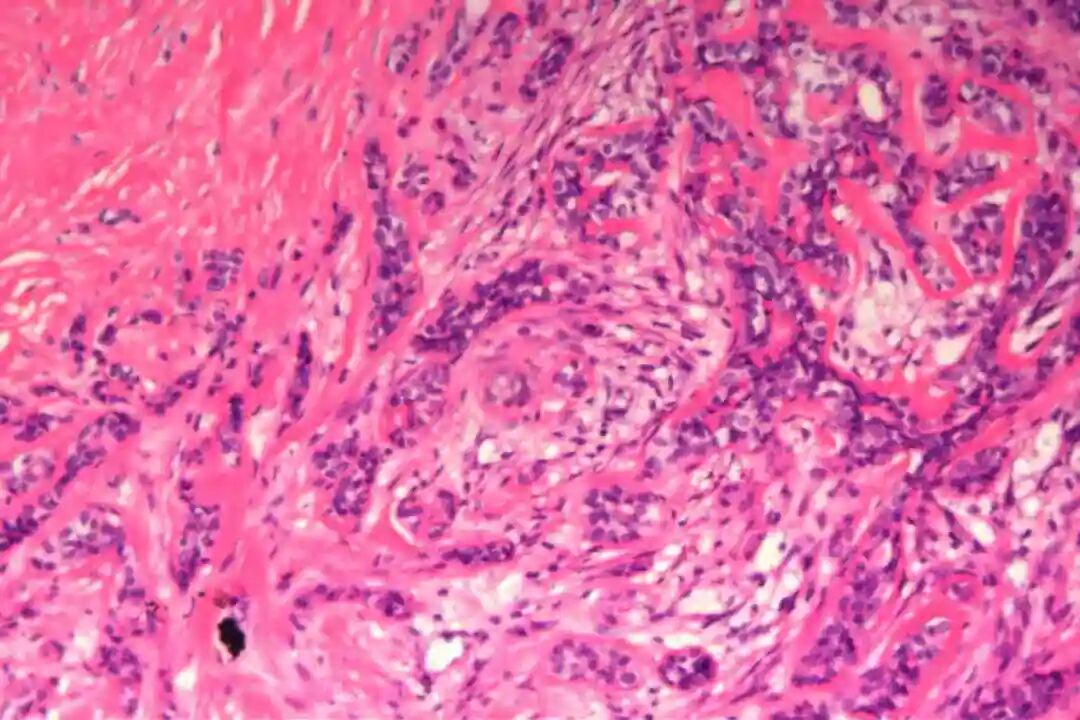
细胞形态:基底样肌上皮细胞体积较小,呈圆形或卵圆形,细胞核深染、染色质均匀,核仁不明显,胞质稀少、淡嗜酸性;腺上皮细胞体积略大,呈柱状或立方状,细胞核淡染、染色质疏松,核仁清晰,胞质丰富、嗜酸性。实性巢团内可见少量微小腔隙,腔隙内可含有少量嗜酸性或嗜碱性黏液样物质(PAS染色阳性),这是实体型与其他实性肿瘤的重要鉴别点;核分裂象少见,一般≤5个/10HPF,部分实体型区域可出现轻度至中度细胞异型性,但无明显恶性增殖活性表现,与高级别乳腺癌的细胞异型性有明显区别。
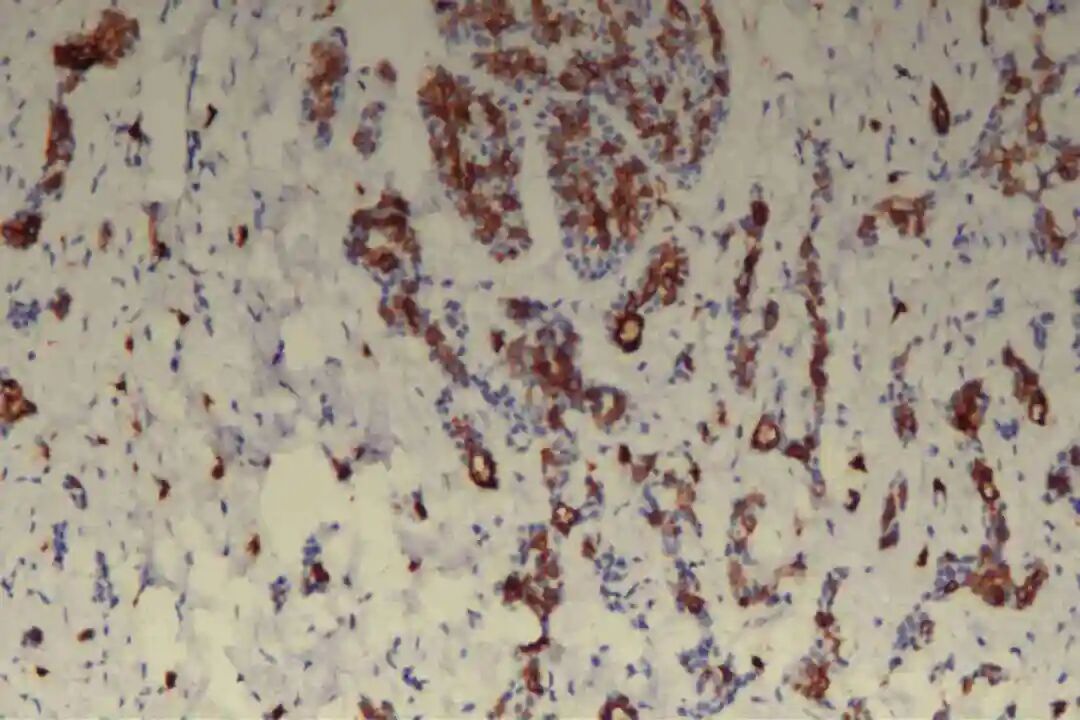
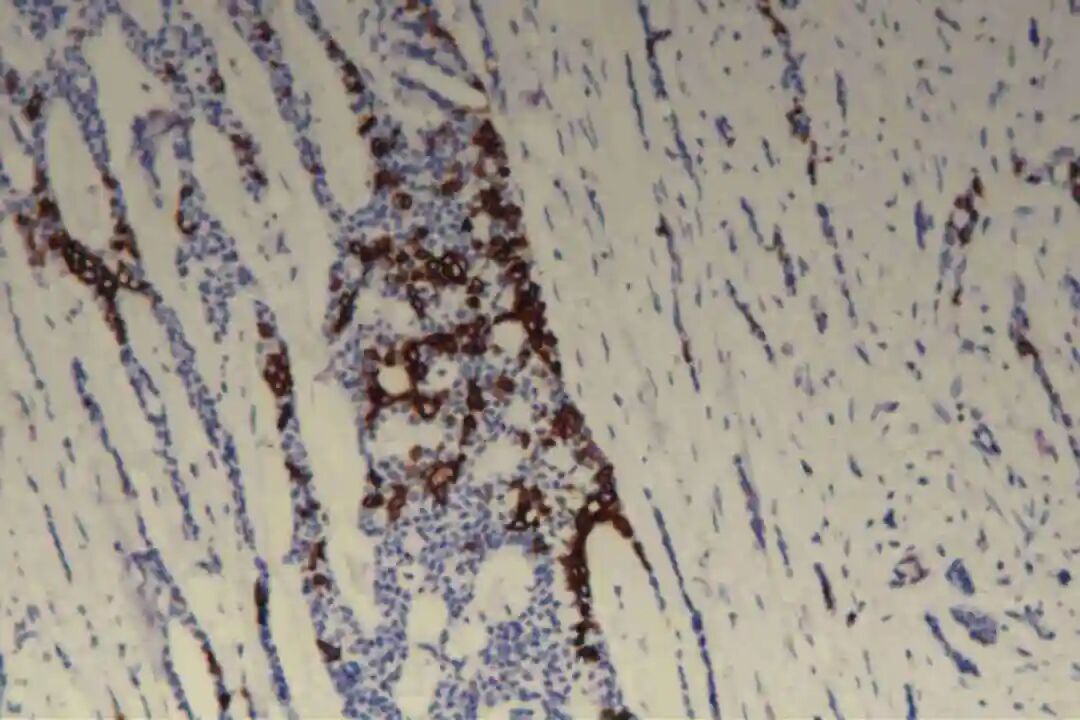
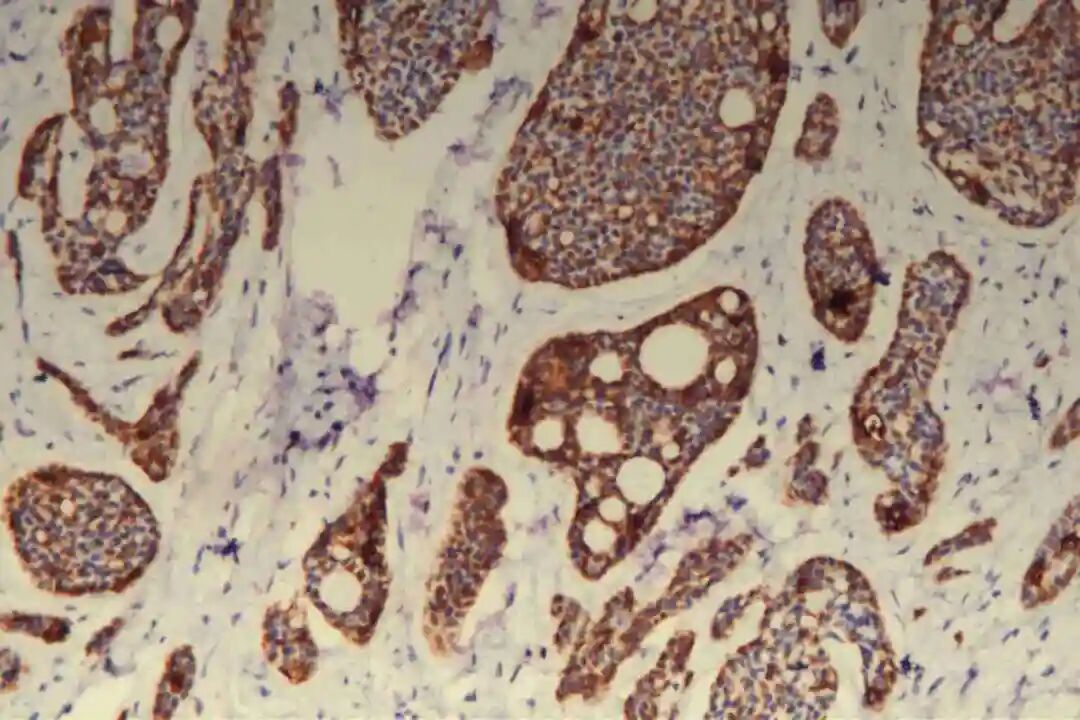
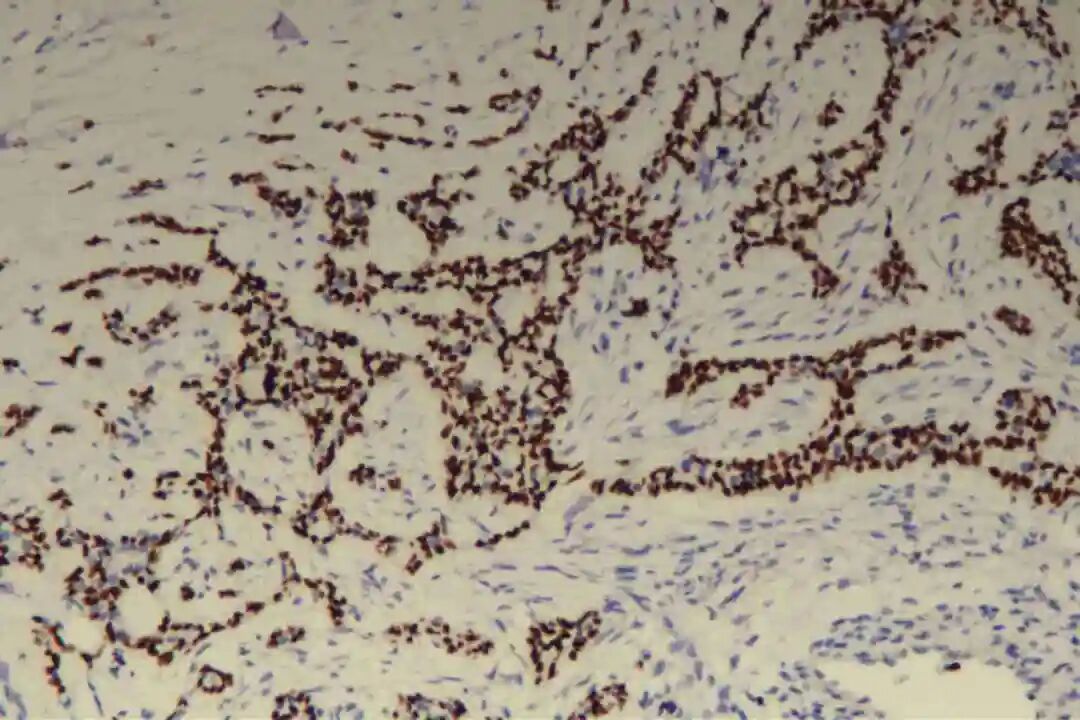
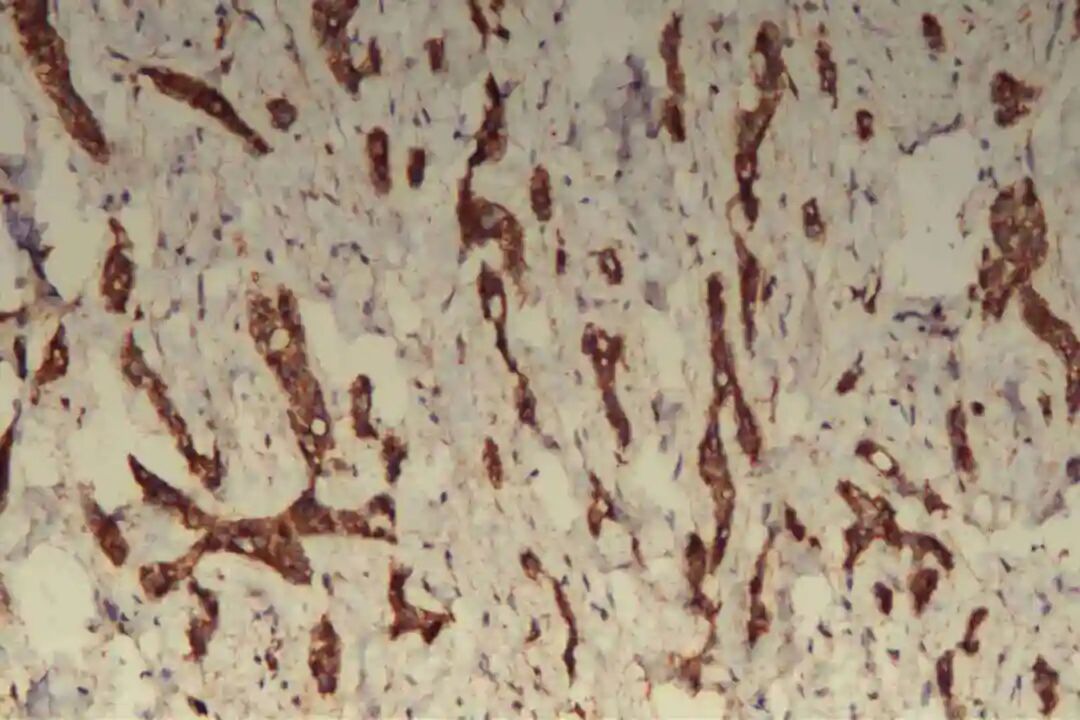
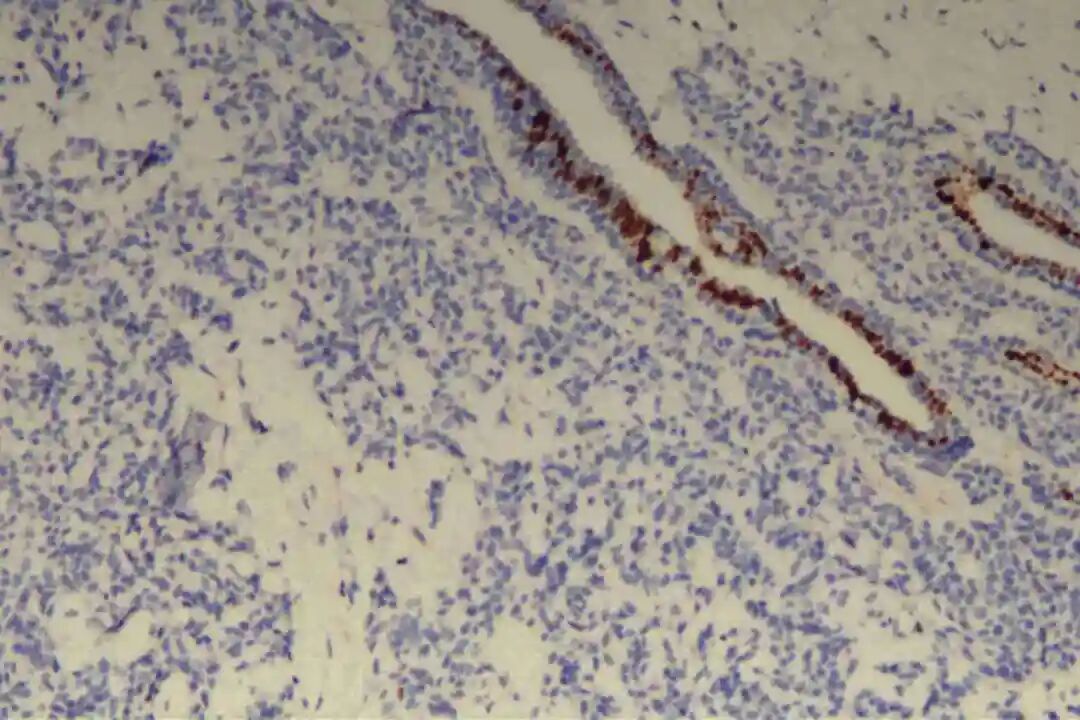
免疫组化:09号片:ER(-),PR(-),Her-2(2+),CK7(腺上皮+),CD117(+),CK5/6(肌上皮+),P63(肌上皮+),GCDFP-15(-),GATA3(-),S-100(+,显示神经侵犯),P120(膜+),E-Cadherin(膜+),P53(野生表型),Ki67(+)10%。
病理诊断:(左)乳腺:符合腺样囊性癌,实体型为主,部分经典型;肿块大小约5.5x4.5x3.2cm,神经见癌侵犯,脉管内未见癌栓;标本上、下、内、外、表面及基底切缘均未见癌;乳头见癌累及。
实体型区域与经典型区域无明显明确界限,相互穿插分布,实体型巢团可逐渐过渡为经典型的筛状或管状结构,两种区域的细胞成分相互延续,均可见腺上皮细胞与肌上皮细胞的混合存在,无明显细胞异型性差异(实体型区域异型性略高于经典型,但整体温和)。这种混合性形态是本病的重要镜下特点,也是与单纯实体型PACC、单纯经典型PACC的主要区别。
腺上皮细胞主要表达细胞角蛋白(CK)家族相关标志物,其中CK7、CK8/18呈弥漫阳性表达,CK19呈局灶性阳性表达,这是确认腺上皮细胞来源的核心依据;部分病例中,腺上皮细胞可表达CD117(c-Kit),呈弥漫或局灶阳性,CD117在实体型区域的阳性表达率高于经典型区域,可作为实体型PACC的辅助鉴别指标。此外,腺上皮细胞不表达雌激素受体(ER)、孕激素受体(PR)及人表皮生长因子受体2(Her-2),即“三阴性”表型,这是PACC与激素受体阳性乳腺癌、Her-2阳性乳腺癌的重要区别,也是临床治疗方案选择的重要依据之一。
肌上皮细胞是PACC的重要组成部分,其标志物表达是诊断PACC的关键,主要表达p63、P40、平滑肌肌动蛋白(SMA)、肌动蛋白(Actin)及S-100蛋白,其中p63、P40呈弥漫阳性表达,SMA、S-100蛋白呈局灶或弥漫阳性表达。
Ki-67增殖指数:整体较低,一般为5%-20%,实体型区域Ki-67指数略高于经典型区域(可达到10%-25%),但均低于其他高危型乳腺癌(如浸润性导管癌,Ki-67指数多≥30%),这与PACC惰性生长的临床特点一致,也是评估预后的重要参考指标。
此外,肿瘤细胞不表达神经内分泌标志物(CgA、Syn、CD56),可排除神经内分泌肿瘤;不表达GCDFP-15,可排除大汗腺来源肿瘤;基底膜物质(Ⅳ型胶原、laminin)阳性,主要分布于筛状结构、管状结构的腔隙周围及实性巢团的微小腔隙内,进一步支持PACC的诊断。
肿瘤体积较大(>3cm)、边界模糊、浸润范围较广,或患者拒绝保乳、乳房体积较小无法行保乳手术的患者,手术方式为切除患侧整个乳房,无需常规行腋窝淋巴结清扫,仅在术前或术中明确腋窝淋巴结转移时,行腋窝淋巴结取样或清扫。
由于该类型PACC具有惰性生长特点,对化疗、内分泌治疗、靶向治疗敏感性较低,辅助治疗仅适用于高危患者。
鉴别诊断:1. 乳腺纤维腺瘤:多见于青年女性(20-30岁),肿块边界清晰、活动度好,质地中等,无乳头异常及皮肤侵犯,镜下可见腺管和纤维组织增生,无浸润性生长,细胞无异性性,免疫组化显示肌上皮细胞标志物(p63、SMA)仅围绕腺管分布,无实性巢团及筛状结构,MYB-NFIB基因融合阴性,可与本病明确鉴别。
2. 乳腺导管扩张症(浆细胞性乳腺炎):多见于中年女性,病程较长,可分为急性、亚急性和慢性期,急性期可表现为乳房硬性肿块、边界不清,伴有皮肤红、肿、热、痛,类似炎性乳腺癌;慢性期可出现乳头溢液、乳头内陷,镜下可见乳腺导管扩张,管内充满脂质物质,周围有浆细胞、淋巴细胞浸润,无腺上皮细胞和肌上皮细胞构成的实性巢团、筛状结构,免疫组化显示ER、PR可阳性,MYB-NFIB基因融合阴性,与本病鉴别不难。
3. 乳管内乳头状瘤:多见于40-50岁女性,主要表现为单侧单孔乳头溢液(多为血性),部分可触及乳晕周边肿块,镜下可见乳腺导管内乳头状突起,由腺上皮细胞构成,无肌上皮细胞增生及实性巢团、筛状结构,免疫组化显示肌上皮细胞标志物仅分布于乳头突起的基底部,无弥漫表达,MYB-NFIB基因融合阴性,可与本病鉴别。
4. 浸润性导管癌(三阴性亚型):多见于中老年女性,肿块质地坚硬、边界模糊,活动度差,乳头异常、皮肤侵犯及腋窝淋巴结转移发生率较高,镜下可见癌细胞呈实性巢团、条索状分布,细胞异型性明显,核分裂象多见,可见坏死,无筛状结构及肌上皮细胞增生,免疫组化显示肌上皮细胞标志物(p63、SMA)阴性或局灶阳性,无MYB-NFIB基因融合,多存在TP53基因突变,Ki-67指数较高(≥30%),可与本病鉴别。此外,浸润性导管癌的远处转移发生率较高,预后较差,与本病的惰性生长特点有明显区别。
5. 乳腺基底样癌:属于三阴性乳腺癌的一种,镜下可见癌细胞呈实性巢团分布,细胞呈基底样特征,与本病实体型区域形态相似,但乳腺基底样癌无肌上皮细胞增生,无筛状结构、管状结构,免疫组化显示肌上皮细胞标志物(p63、SMA)阴性,MYB-NFIB基因融合阴性,多存在BRCA1基因突变,Ki-67指数较高,局部复发率和远处转移率均高于本病,可通过免疫组化及分子病理检查明确鉴别。
6. 乳腺黏液腺癌:多见于老年女性,肿块边界清晰、质地较软,镜下可见大量黏液池,癌细胞漂浮于黏液池中,形成腺样结构,无实性巢团及筛状结构,免疫组化显示ER、PR多为阳性,MYB-NFIB基因融合阴性,与本病(ER、PR阴性,有实性巢团、筛状结构)鉴别不难。此外,乳腺黏液腺癌的超声表现多为无回声或低回声,伴有黏液性暗区,与本病的实性肿块表现有明显区别。
6. 乳腺神经内分泌癌:镜下可见癌细胞呈巢团状、条索状分布,细胞呈圆形或卵圆形,类似本病实体型区域,但乳腺神经内分泌癌表达神经内分泌标志物(CgA、Syn、CD56),无肌上皮细胞增生及筛状结构,免疫组化显示肌上皮细胞标志物阴性,MYB-NFIB基因融合阴性,可与本病鉴别。此外,乳腺神经内分泌癌的远处转移发生率较高,预后较差,与本病的惰性生长特点有明显区别。
7. 乳腺肌上皮癌:镜下主要以肌上皮细胞增生为主,形成实性巢团,无腺上皮细胞增生,无筛状结构、管状结构,免疫组化显示肌上皮细胞标志物(p63、SMA)弥漫强阳性,腺上皮细胞标志物(CK7、CK8/18)阴性,MYB-NFIB基因融合阴性,可与本病鉴别(本病有腺上皮细胞和肌上皮细胞双重增生,腺上皮细胞标志物阳性)。
8. 乳腺腺样囊性癌与涎腺腺样囊性癌转移鉴别:涎腺腺样囊性癌多发生于腮腺、颌下腺,可转移至乳腺,镜下形态与乳腺原发性腺样囊性癌相似,但涎腺腺样囊性癌多有涎腺原发灶病史,免疫组化显示GCDFP-15阴性(乳腺原发性PACC也阴性),需通过病史、影像学检查(排查涎腺原发灶)及分子病理检查进一步鉴别,两者均存在MYB-NFIB基因融合,但涎腺腺样囊性癌的实体型成分少见,多以经典型为主,可辅助鉴别。
目前,对于该类型PACC的研究仍存在不足,尤其是实体型成分的发生机制、NOTCH1基因突变的具体作用、靶向治疗药物的研发等方面,仍需更多临床病例积累和基础研究探索。随着分子病理技术的不断发展,MYB-NFIB基因融合检测、NOTCH1基因突变检测等将更加普及,有望为该类型PACC的精准诊断、个体化治疗及预后评估提供更可靠的依据,进一步改善患者的治疗效果和生活质量。